Individualizirano testiranje minimalne rezidualne bolesti (MRD) kod raka mokraćnog mjehura.
Pomaže u detekciji ranih znakova povrata bolesti prije konvencionalnih slikovnih pretraga, u identifikaciji bolesnika koji mogu imati korist od dodatnog liječenja te u procjeni terapijskog odgovora¹–³.

Nakon povrata raka mokraćnog mjehura, Bonnie i njezin liječnik koristili su Signatera™ za praćenje učinkovitosti imunoterapijskog liječenja. Testiranje testom Signatera™ pomoglo je u usmjeravanju važnih odluka o promjeni liječenja te je Bonnie pružilo osjećaj sigurnosti.
„Dobivanje rezultata [Signatera™] pružilo mi je sigurnost da mogu uživati u životu.” – Bonnie Miller


DNK iz stanica vašeg tijela, i tumorskih i zdravih, može se naći u krvi.

Signatera™ koristi jedinstveni molekularni potpis tumora za detekciju tumorskog DNK u krvi.

Sljedeći put kada posjetite onkologa, pitajte ga može li Vam Signatera pomoći.
Nakon svakog uzorkovanja krvi za test Signatera™, liječnik zaprima izvješće koje navodi je li cirkulirajući tumorski DNK (ctDNA) detektiran u krvi. Izvješće također prikazuje promjene razina ctDNA tijekom vremena. Rezultate testa Signatera™ uvijek treba tumačiti liječnik.

Ako je bolest dijagnosticirana u ranom stadiju, takav nalaz povezan je s većom vjerojatnošću odsutnosti znakova bolesti.
U bolesnika s metastatskom bolešću, negativan rezultat može upućivati na to da je liječenje smanjilo broj proliferirajućih tumorskih stanica te snizilo razinu tumorskog DNK ispod granice detekcije. To može biti pokazatelj terapijskog učinka.

Pozitivan rezultat ukazuje na to da je tumorski DNK detektiran u krvi te je, u bolesnika s ranostadijskom bolešću, povezan s povećanim rizikom povrata bolesti. Liječnik može nastaviti pratiti razine ctDNA radi procjene terapijskog odgovora tumora.

Porast razine ctDNA tijekom vremena može upućivati na rast ili širenje bolesti.
Pad razine ctDNA tijekom vremena može upućivati na smanjenje tumorskog opterećenja ili odgovor na liječenje.
Stručni uvidi o praćenju tumora i ranoj detekciji recidiva
1Coombes RC, et al. Clin Cancer Res. 2019 Jul 15;25(14):4255-4263.
2Magbanua MJM, et al. Ann Oncol. 2021; 32(2):229-239.
3Magbanua MJM, et al. Comparison of the predictive and prognostic significance of circulating tumor DNA in patients with high risk HER2-negative breast cancer receiving neoadjuvant chemotherapy. AACR; April 8-13, 2022.
4Cutts R, et al. Detection of ctDNA following surgery predicts relapse in breast cancer patients receiving primary surgery. SABCS; December 7-11, 2021.
5Shaw JA, et al. Serial postoperative ctDNA monitoring for early detection of breast cancer recurrence. ASCO; June 3-7, 2022.
6Bratman SV, et al. Nature Cancer. 2020;1(9):873-881.
Poboljšano preživljenje bez bolesti (DFS) i ukupno preživljenje (OS) zabilježeno je kod Signatera™-pozitivnih pacijenata liječenih adjuvantnom imunoterapijom.¹˒²
Serijski Signatera™-negativni pacijenti imali su izvrsne ishode preživljenja i bez adjuvantne terapije.
Faza 3 ispitivanja IMvigor011 pokazala je da su Signatera™-pozitivni pacijenti liječeni adjuvantnim atezolizumabom postigli statistički značajna i klinički relevantna poboljšanja ishoda preživljenja:

Signatera™ MRD test validiran je u dva ključna adjuvantna ispitivanja faze 3 u MIBC-u, pokazujući kako personalizirano MRD testiranje može sigurno proširiti adjuvantni terapijski prozor.

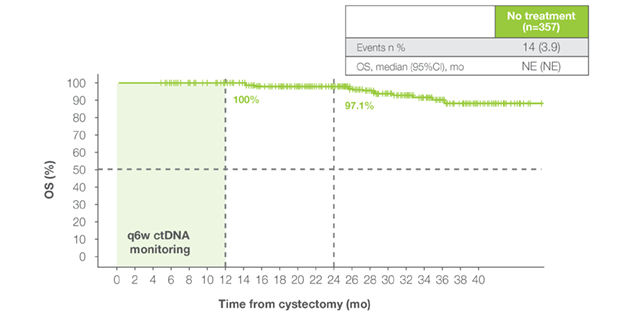
Pacijenti koji su nakon cistektomije ostali serijski Signatera™-negativni postigli su iznimne ishode:
• stope ukupnog preživljenja (OS) od 100% nakon 12 mjeseci i 98% nakon 18 mjeseci¹
• stope preživljenja bez bolesti (DFS) od 92% nakon 12 mjeseci i 88% nakon 18 mjeseci¹

Signatera™-pozitivnost u jednom vremenskom trenutku nakon cistektomije može predvidjeti koji će pacijenti imati korist od adjuvantne imunoterapije.¹˒⁴

Rana dinamika ctDNA može pomoći u predviđanju koristi od imunoterapije.³

Signatera™ ctDNA status prije neoadjuvantne kemoterapije, prije cistektomije i nakon cistektomije bio je snažno prognostički povezan s ishodima pacijenata.²

Kod ovog pacijenta s mišićno invazivnim rakom mokraćnog mjehura, serijsko Signatera™ testiranje pokazuje da promjene razine ctDNA mogu pomoći u procjeni odgovora na adjuvantno liječenje:

Signatera™ MRD testiranje nakon definitivnog liječenja može identificirati molekularni povrat bolesti prije radiološki vidljivog relapsa. Rezultati kliničke studije objavljene u Journal of Clinical Oncology pokazali su sljedeće:

Promjene razina ctDNA, procijenjene serijskim Signatera™ testiranjem u kombinaciji sa slikovnim pretragama, mogu pomoći u procjeni odgovora na imunoterapiju. Za ovog pacijenta koji je započeo liječenje pembrolizumabom:³

Časopis: New England Journal of Medicine
Godina: 2025
Časopis: Annals of Oncology
Godina: 2025
Časopis: Molecular Oncology
Godina: 2020
Gschwend JE, Assaf ZJ, Mariathasan S, et al. Overall survival by circulating tumor DNA status in patients with post-operative muscle-invasive urothelial carcinoma treated with atezolizumab: Update from IMvigor010. EAU, Amsterdam, Netherlands, July 1-4, 2022.
Powles T, Young A, Nimeiri H, et al. Molecular residual disease (MRD) detection with a tissue comprehensive genomic profiling (CGP)-informed personalized monitoring assay: An exploratory analysis of the IMvigor010 observation arm. ASCO Genitourinary Cancer Symposium, San Francisco, CA. Feb 17-19, 2022.
Birkenkamp-Demtröder K, Christensen E, Sethi H, et al. Sequencing of Plasma cfDNA from Patients with Locally Advanced Bladder Cancer for Surveillance and Therapeutic Efficacy Monitoring. Poster presented at: European Society for Medical Oncology; October 19-23, 2018; Munich, Germany.
Birkenkamp-Demtröder K, Christensen E, Sethi H, et al. Sequencing of Plasma cfDNA from Patients with Locally Advanced Bladder Cancer for Surveillance and Therapeutic Efficacy Monitoring. Poster presented at: American Association for Cancer Research; April 14-18, 2018; Chicago, IL.
Nedavna serija prospektivnih studija procjenjivala je može li Signatera™ poboljšati otkrivanje povrata bolesti i procjenu odgovora na liječenje kod pacijenata s rakom testisa.
Signatera™ je otkrila povrat raka testisa uz 96% specifičnosti i 87% negativne prediktivne vrijednosti (NPV) u usporedbi sa slikovnim metodama u stadiju I bolesti te je s 100% točnošću predvidjela progresiju u post-RPLND MRD okruženju.

1Powles T, Kann AG, Castellano D, et al. ctDNA-Guided Adjuvant Atezolizumab in Muscle-Invasive Bladder Cancer.New England Journal of Medicine. Published online October 20, 2025. doi:10.1056/NEJMoa2508652.
2Galsky MD, Gschwend JE, Milowsky MI, et al. Adjuvant Nivolumab Versus Placebo for High-Risk Muscle-Invasive Urothelial Carcinoma: 5-Year Efficacy and ctDNA Results from CheckMate 274. Annals of Oncology. Published online October 17, 2025. doi:10.1016/j.annonc.2025.09.139.
3Bratman SV, Yang SYC, Iafolla MAJ, et al. Personalized circulating tumor DNA analysis as a predictive biomarker in solid tumor patients treated with pembrolizumab. Nature Cancer. 2020;1:873-881. doi:10.1038/s43018-020-0096-5.
4Powles T, et al. European Urology. 2023; https://doi.org/10.1016/j.eururo.2023.06.007.
5Powles T, et al. Presented at EAU annual conference, 2024.
6American Cancer Society. Key statistics for testicular cancer. 2025. Available at: https://www.cancer.org/cancer/types/testicular-cancer/about/key-statistics.html
7Reuben Ben-David, et al. Utility of tumor-informed circulating tumor DNA (ctDNA) in patients undergoing retroperitoneal lymph node dissection for testicular cancer. Icahn School of Medicine at Mount Sinai. Poster presented in 2023.
8Parth Thakker, et al. Circulating tumor DNA as a prognostic biomarker to predict retroperitoneal histology in patients undergoing retroperitoneal lymph node dissection. Indiana University. Poster presented at ASCO GU, 2025.
9Reuben Ben-David, et al. Comparative performance of tumor-informed circulating tumor DNA and imaging studies in monitoring patients with Stage I testicular cancer. Icahn School of Medicine at Mount Sinai. Poster presented at ASCO GU, 2024.