Signatera™ za rak dojke
Signatera™ je tumor informativni test molekularne rezidualne bolesti (MRD) koji kod raka dojke može pomoći u odlukama o skrbi pacijenta.
Nadziri svoj rak dojke
Signatera test za otkrivanje rezidualne bolesti je za specifični tumor napravljen test za osobe kojime je dijagnosticiran rak dojke ili neki drugi solidni tumor. Signatera može otkriti ostatnu bolest (MRD) u obliku cirkulirajućih tumorskih DNK-malih odlomaka DNK ispuštenih iz stanica tumora.

Kada Vaš doktor naruči prvu Signateru, tkivo tumora i uzorak krvi šalju se u Natera laboratorij. U Natera laboratoriju će iz vašeg zaprimljenog tkiva stručnjaci raditi na tome da izoliraju vaše tumorsko tkivo.

Nakon što je vaš test napravljen, vaša krv biti će poslana svaki put kad se ponovo naruči Signatera.

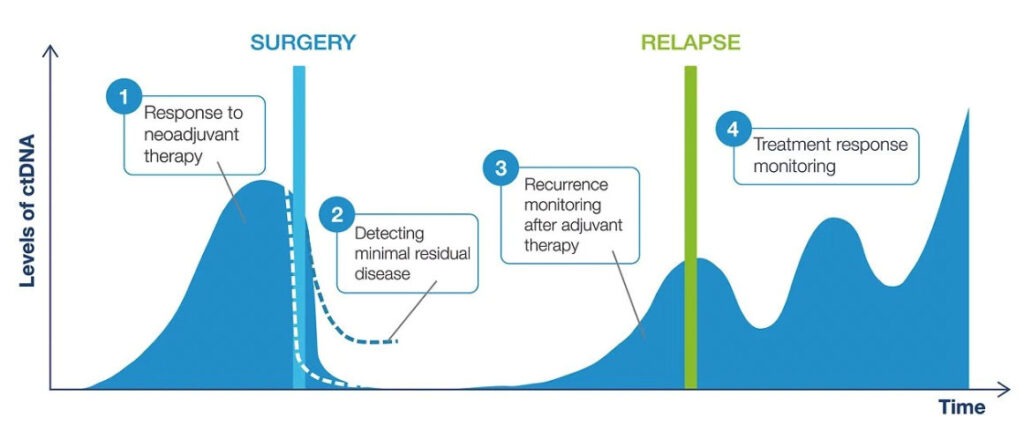
Opetovano testiranje Signaterom može pokazati promjene u vašoj količini ctDNK, pomažući vašem doktoru razumijeti smanjujeli se vaš rak, raste li, ili se vraća.
Informiraj se o svome planu liječenja
Ako vi ili netko vaš ima dijagnosticiran rak dojke, vjerojatno imate mnogo pitanja. Signatera uz ostale testove vama i vašem doktoru pomaže poduzimanju sljedećih koraka i vodi ka informiraniroj odluci.

Testiranje Signatere nakon operacije i/ili inicijalne terapije može vašem doktoru pomoći u otkrivanju ostatnih tragova bolesti raka u vašem tijelu. Takva informacija može vama i vašem doktoru razumijeti rizik za recidiv, pomoći u odluci oko terapije i isplanirati strategiju nadzora.1-4

- Signatera može pružiti rano upozorenje da se vaš rak dojke možda vraća na molekularnoj razini.
- Kliničke studije pokazale su da za osobe s visokim rizikom za rak dojke Signatera može prepoznati recidiv prije nego bude vidljiv na scanu.5
- Ranije otkrivanje recidiva može vašem doktoru dati više mogućnosti za planiranje i razvijanje plana vaše skrbi.

- Signatera može procijeniti raste li ili pada razia ctDNK tijekom terapije, pomažući vašem doktoru razumijeti djeluje li terapija.
- Signatera se preporučuje za nadzor raka dojke stadija II-IV u neoadjuvantnoj terapiji, za nadzor odgovora na immune-checkpoint inhibitor (ICI) terapiju ili imunoterapije i za pacijente sa solidnim tumorom.
Iskustvo pacijenta - Danijelina priča
Kada je Signatera otkrila molekularni recidiv njezinog raka dojke, ona i njezin doktor morali su brzo reagirati.
“Informacije i znanje su moć – tako se pobjeđuje rak”.
Danijelina priča podcrtava važnost zauzimanja za sebe i kako korištenje potrebnih alata čine razliku.
Blog
Stručni uvidi o praćenju tumora i ranoj detekciji recidiva
Reference
1Coombes RC, et al. Clin Cancer Res. 2019 Jul 15;25(14):4255-4263.
2Magbanua MJM, et al. Ann Oncol. 2021; 32(2):229-239.
3Magbanua MJM, et al. Comparison of the predictive and prognostic significance of circulating tumor DNA in patients with high risk HER2-negative breast cancer receiving neoadjuvant chemotherapy. AACR; April 8-13, 2022.
4Cutts R, et al. Detection of ctDNA following surgery predicts relapse in breast cancer patients receiving primary surgery. SABCS; December 7-11, 2021.
5Shaw JA, et al. Serial postoperative ctDNA monitoring for early detection of breast cancer recurrence. ASCO; June 3-7, 2022.
6Bratman SV, et al. Nature Cancer. 2020;1(9):873-881.
Informirane odluke za pacijente visokog rizika
Procjena rizika pacijenta
Identifikacija pacijenata visokog rizika s ostatnom bolesti nakon operacije koji bi mogli imati korist od adjuvantne terapije
5.6x
viši rizik od udaljenih metastaza kod pacijenata s ostatnom bolesti (MRD) nakon operacije.
Rana detekcija povrata bolesti
Signatera serijskim testiranjem nadgleda se i identificira rak dojke pacijenta s visokim rizikom za recidiv
52x
viši rizik od recidiva kod pozitivnog ctDNA u odnosu na negativni ctDNA
Procjena terapijskog odgovora
Praćenjem promjena u količini ctDNA procjenjuje se terapijski odgovor
6 tjedana
Za procjenu odgovora na imunoterapiju
SignateraTM Genome demonstrated ultrasensitive MRD detection down to 1 part per million (PPM)11

Pokazalo se da SignateraTM ima visoku prognostičku vrijednost za ishod pacijenata i prediktivnu vrijednost za korist od adjuvantnog liječenja.
Signatera™ Genome: Evolucija MRD testiranja iz najpouzdanijeg testa za rak dojke
Kako Natera nastavlja biti predvodnik u preciznoj onkologiji, Signatera™ Genome pokazao je izvanredne rezultate u liječenju raka dojke, nudeći nenadmašnu osjetljivost i specifičnost u detekciji rezidualne bolesti te pružajući ključne informacije za donošenje važnih odluka o liječenju.
Rana detekcija povrata bolesti
- Do 30 % pacijentica s rakom dojke, koje nakon liječenja s
namjerom izlječenja nemaju dokaza o bolesti, na kraju će
doživjeti povrat bolesti i preminuti od nje4 — što ukazuje da postojeći alati nisu dovoljno učinkoviti u ranom otkrivanju recidiva prije nego što pacijentice postanu simptomatske. - Približno 10-15 % pacijentica doživi smanjenje općeg stanja i
funkcionalnosti pri povratu bolesti, a mogućnosti liječenja su
tada ograničene5. - Longitudinalno testiranje s SignateraTM dokazano identificira
pacijentice s visokim rizikom od povrata bolesti s
osjetljivošću od 88 % i u medijanu 10,5 mjeseci (raspon 0-38
mjeseci) prije detekcije slikovnim metodama2, što
potencijalno omogućuje pravovremenu i učinkovitu
intervenciju.

Ključna pitanja tijekom liječenja raka dojke

Istražite podatke o raku dojke
Shema studije I-SPY 2
Studije I-SPY 2: Može li ctDNA preciznije odrediti vrijednost pCR-a kao surogatnog pokazatelja preživljenja?
Kod pacijentica liječenih neoadjuvantnom terapijom postizanje patološkog kompletnog odgovora (pCR) općenito upućuje na povoljnu prognozu. No kako stratificirati rizik kod pacijentica s rezidualnom bolešću?
Ciljevi ctDNA analize u studiji I-SPY 2
- Procijeniti ctDNA kao biomarker za praćenje odgovora na neoadjuvantnu terapiju.⁶˒⁷
- Procijeniti prognostičku vrijednost ctDNA u stratifikaciji pacijentica prema riziku ranog metastatskog povrata bolesti.⁶˒⁷
Glavni platformski protokol studije I-SPY 2

- Odgovor na neoadjuvantnu kemoterapiju (NAC) i ispitivane terapije procjenjivan je praćenjem dinamike ctDNA u četiri vremenske točke.
- ctDNA iz plazme analizirana je u četiri vremenske točke: prije početka liječenja (T0), 3 tjedna nakon uvođenja paklitaksela/ispitivanog lijeka (T1), između režima s paklitakselom/ispitivanim lijekom i antraciklinskog režima (T2) te prije operacije (T3).
Rezultati studije I-SPY 2
Koncentracija ctDNA (MTM/ml) pri dijagnozi bila je povezana s većim rizikom od povrata bolesti, neovisno o podtipu receptora.
Studijska kohorta:
712 pacijentica s visokorizičnim ranim rakom dojke: HR+/HER2–, TNBC i HER2+ bolest
MRD testiranje i utjecaj na DRFS:
Pacijentice bez detektabilne ctDNA prije neoadjuvantne terapije imale su trogodišnje DRFS od 96,8 %.


- Pacijentice koje su postigle pCR i eliminirale ctDNA imale su najbolje ishode preživljenja, dok su najlošije ishode imale one koje nisu postigle pCR i bile su ctDNA-pozitivne.¹–³
- Neovisno o statusu pCR-a, perzistentna ctDNA-pozitivnost u vremenskoj točki T3 bila je povezana s kraćim DRFS-om u usporedbi s ctDNA-negativnošću.¹–³
Procjena rizika kod pacijentica nakon operacije radi prepoznavanja onih s rezidualnom bolešću koje mogu imati korist od intenzivnijeg ili produljenog adjuvantnog liječenja
Studija EBLIS: ctDNA status, u kombinaciji s postojećim alatima nakon operacije i adjuvantne kemoterapije, omogućio je prepoznavanje pacijentica visokog rizika s nepovoljnijim preživljenjem8 bez povrata bolesti, koje bi mogle imati korist od adjuvantnog liječenja za visokorizične bolesnice.

Studija I-SPY 2: Prije operacije pokazano je da perzistencija ctDNA, neovisno o statusu pCR-a, omogućuje prepoznavanje pacijentica sa slabijim odgovorom na neoadjuvantnu kemoterapiju i visokim rizikom od recidiva, što može pridonijeti donošenju odluka o adjuvantnom liječenju.

Studija ranog raka dojke: U analizu je uključeno 48 pacijentica s ranim rakom dojke liječenih primarnim kirurškim zahvatom, od kojih je 40 primilo i kemoterapiju; ukupno su prikupljena 144 uzorka plazme. Medijan praćenja iznosio je 5 godina (0,5–6)1.

- 38 % pacijentica koje su nakon operacije bile ctDNA-pozitivne doživjelo je recidiv, dok su preostale možda imale korist od adjuvantnog liječenja.¹
- Detekcija ctDNA nakon operacije bila je povezana s lošijim ishodima u usporedbi s izostankom detekcije ctDNA (DMFS HR 5,6; 95 % CI 1,1–29,3; P = 0,04).¹
- Ovi podaci sugeriraju da je MRD-pozitivnost nakon operacije prognostički nepovoljan čimbenik, ali i potencijalno podložna promjeni adjuvantnim liječenjem.¹

Studija DARE: pružila je uvid u ulogu ctDNA u usmjeravanju odluka o adjuvantnom liječenju kod visokorizičnog ranog raka dojke
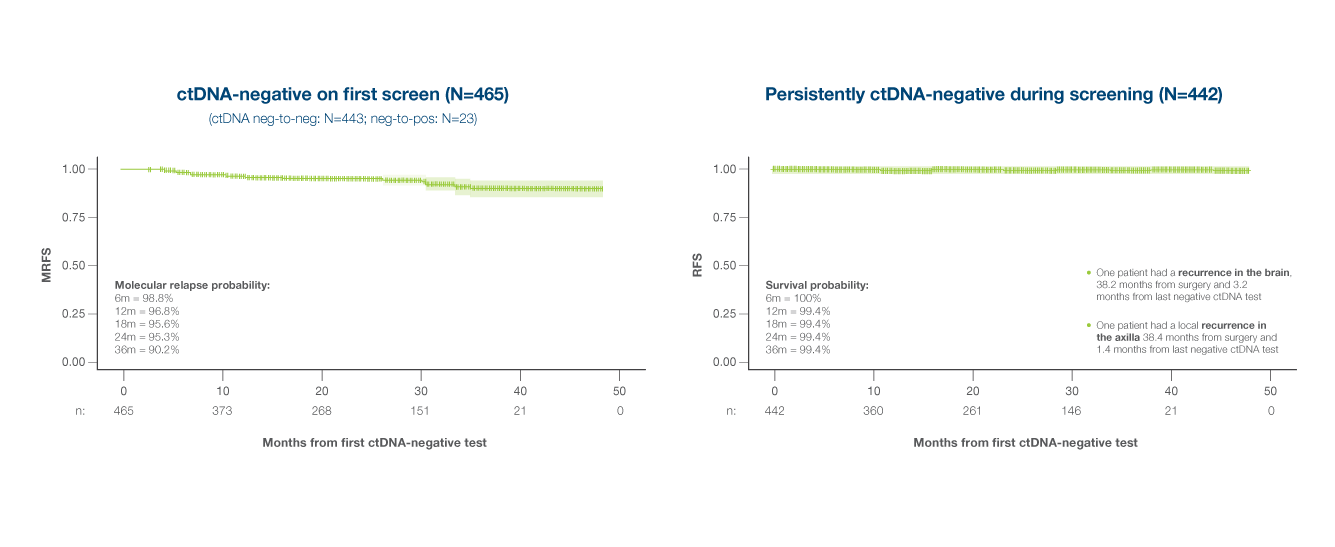
- Tijekom praćenja ctDNA-pozitivnost utvrđena je u 12 % pacijentica.⁹
- U 73 % ctDNA-pozitivnih pacijentica slikovne metode nisu pokazivale metastatsku bolest (tj. radilo se o molekularnom relapsu).⁹
- Među pacijenticama s molekularnim relapsom, 93 % bilo je spremno na randomizaciju.⁹
- ctDNA-negativnost bila je snažno povezana s boljim preživljenjem bez povrata bolesti (RFS), uz negativnu prediktivnu vrijednost od 99 % pri medijanu praćenja od 27,4 mjeseca.⁹
Povezanost ranih promjena ctDNA tijekom liječenja s RFS-om
- Klinički relaps zabilježen je u 1 od 9 pacijentica koje su 3 mjeseca nakon randomizacije imale eliminaciju ctDNA ili smanjenje njezine razine.
- Klinički relaps zabilježen je u 6 od 10 pacijentica s porastom razine ctDNA.

Studija EBLIS: Postoji li osjetljivija tehnologija koja može ranije otkriti povrat bolesti?
Exploratory Breast Lead Interval Study (EBLIS) ispitivala je potencijalnu primjenu praćenja ctDNA u pacijentica s visokorizičnim rakom dojke u dosad najduljem ispitivanju praćenja ctDNA.
Protokol studije EBLIS

Rezultati studije EBLIS
Test Signatera™ može se primjenjivati serijski za praćenje i prepoznavanje pacijentica s rakom dojke koje imaju visok rizik od povrata bolesti.


- Praćeno je 156 pacijentica tijekom razdoblja od 12 godina, uključujući sve podtipove raka dojke.
- Osjetljivost od 88 %: test Signatera™ detektirao je ctDNA u 30 od 34 pacijentice prije kliničkog ili radiološkog relapsa.
U dosad najvećoj analizi ctDNA u HR+/HER2– lobularnom raku dojke (n = 7.381), ctDNA-pozitivnost bila je povezana s većim rizikom od povrata bolesti i ranijim relapsom.
Istaknuti podaci: Signatera™ donosi veću jasnoću u procjenu rizika kod lobularnog raka dojke.¹
- 7.381 pacijentica: riječ je o najvećem stvarnom kliničkom istraživanju lobularnog raka dojke u kojem su analizirani ishodi povezani s ctDNA.
- Rani povrat bolesti: unutar dvije godine od operacije ctDNA-pozitivnost identificirala je agresivniju bolest u svim podtipovima, uključujući HR+/HER2– lobularni rak dojke.
- Nakon 2 godine: ctDNA-pozitivnost nastavila je identificirati pacijentice s rizikom od kasnog relapsa, što je obilježje lobularnog raka dojke.
Studija INSPIRE: može li se ctDNA validirati kao rani biomarker odgovora na liječenje inhibitorima imunoloških kontrolnih točaka (ICI)?
Unatoč znatnom napretku u liječenju raka primjenom protutijela koja blokiraju proteine imunoloških kontrolnih točaka, manje od 20 % pacijentica i pacijenata koji ispunjavaju kriterije ostvaruje trajan odgovor ili kliničku korist od inhibitora imunoloških kontrolnih točaka (ICI).⁷ Kako ctDNA može pouzdano identificirati one koji imaju korist od liječenja ICI-jem?
Ciljevi studije INSPIRE
Prospektivno ispitivanje faze II INSPIRE bavilo se klinički relevantnim pitanjima praćenja odgovora na ICI procjenom početnog ctDNA statusa i dinamike ctDNA.
Protokol studije INSPIRE

Rezultati studije INSPIRE
Signatera™ predviđa korist od imunoterapije već u 6. tjednu.
Početna koncentracija ctDNA i dinamika ctDNA tijekom liječenja bile su povezane s preživljenjem bez progresije bolesti (PFS), ukupnim preživljenjem (OS), kliničkim odgovorom i kliničkom koristi.³
- Smanjenje razine ctDNA od početne vrijednosti do početka 3. ciklusa snažan je prediktor duljeg OS-a i PFS-a.³
- Eliminacija ctDNA u bilo kojoj vremenskoj točki bila je povezana s boljim kliničkim ishodima. Svih 12 pacijenata koji su tijekom liječenja imali eliminaciju ctDNA u barem jednoj vremenskoj točki ostalo je živo tijekom razdoblja praćenja (medijan praćenja nakon prve eliminacije iznosio je 25,4 mjeseca).³

U metastatskoj bolesti dinamika ctDNA pokazala se prediktorom odgovora na liječenje u mBC-u.
- Cilj istraživanja bio je ispitati povezanost ranih promjena ctDNA tijekom liječenja s ishodima u stvarnoj kliničkoj praksi.
- U tu je svrhu korištena baza podataka iz stvarne kliničke prakse, povezana s administrativnim podacima o potraživanjima, kako bi se procijenila povezanost između dinamike ctDNA i vremena do sljedeće linije liječenja (TTNT) u 616 pacijentica s mBC-om.¹⁰

Preciznija stratifikacija rizika u ranom (eBC) HR+/HER2– raku dojke
Negativan nalaz testa Signatera™ na razini genoma identificira velik udio ispitivane populacije s iznimno niskim rizikom od povrata bolesti.
Studija PALLAS:
- Pozitivan nalaz testa Signatera™ u C1D1 bio je povezan s anualiziranim rizikom udaljenog recidiva od oko 15 %, dok je negativan nalaz bio povezan s rizikom od oko 1,4 %.
- Stratifikacija rizika prema statusu testa Signatera™ ostala je postojana tijekom vremena te je izdvojila podskupinu visokog rizika s pozitivnim bazalnim nalazom, unatoč općenito niskoj stopi pozitivnosti u HR+/HER2– bolesti.
- Većina pacijentica započela je endokrinu terapiju prije uzimanja uzorka krvi u vremenskoj točki C1D1, pri čemu je približno 80 % njih započelo liječenje prije samog uzorkovanja.

Rano otkrivanje moždanih metastaza u raku dojke primjenom praćenja ctDNA
- U 83 % pacijentica koje su razvile moždane metastaze ctDNA je bila detektabilna prije kliničkog relapsa.
- Kod 62 % pacijentica s metastazama ograničenima samo na mozak ctDNA je bila pozitivna prije postavljanja dijagnoze
- Medijan vremena prednosti od detekcije ctDNA do klinički potvrđene moždane metastaze iznosio je 10 mjeseci.
- Niže razine ctDNA zabilježene su pri relapsu ograničenom samo na mozak u usporedbi s ekstrakranijskom metastatskom bolešću, što upućuje na biološke razlike u otpuštanju tumorske DNA.
Praćenje radi otkrivanja povrata raka dojke, uključujući moždane metastaze
- Pozitivan nalaz ctDNA često je prethodio radiološki ili simptomatski manifestnim moždanim metastazama, čak i kada je mozak bio prvo sijelo povrata bolesti.
- Detekcija ctDNA u kliničkoj je praksi potaknula daljnju slikovnu obradu, što podupire njezinu ulogu kao ranog pokazatelja rizika tijekom praćenja.
- Nalazi upućuju na to da praćenje ctDNA može pomoći u prepoznavanju pacijentica koje bi mogle imati korist od ranije evaluacije središnjega živčanog sustava.

Reference
1Cutts R, et al. Detection of ctDNA following surgery predicts relapse in breast cancer patients receiving primary surgery. SABCS; December 7-11, 2021.
2Shaw JA, et al. Serial postoperative ctDNA monitoring for early detection of breast cancer recurrence. ASCO; June 3-7, 2022.
3Bratman SV, et al. Nature Cancer. 2020;1(9):873-881.
4Early Breast Cancer Trialists’ Collaborative Group. Lancet. 2005;365:1687-1717.
5O’Connor T, et al. Clin Adv Hematol Oncol. 2013;11(6):341-347.
6Magbanua MJM, et al. Ann Oncol. 2021; 32(2):229-239.
7Magbanua MJM, et al. Comparison of the predictive and prognostic significance of circulating tumor DNA in patients with high risk HER2-negative breast cancer receiving neoadjuvant chemotherapy. AACR; April 8-13, 2022.
8Coombes RC, et al. Clin Cancer Res. 2019 Jul 15;25(14):4255-4263.
9Lajos Pusztai, et al. Circulating tumor (ct)DNA monitoring of ER+/HER2- high-risk breast cancer during adjuvant endocrine therapy. Presented at the American Society Clinical Oncology annual meeting; 2025; Abstract 1010.
10Pedram Razavi, et al. Circulating tumor DNA (ctDNA) dynamics as a predictor of treatment response in metastatic breast cancer (mBC). Presented at the American Society Clinical Oncology annual meeting; 2025; Abstract 1011.
11George et al. (2025, May 30–June 3). Clinical performance of Signatera Genome assay in a cohort of patients (pts) with solid tumors [Poster presentation]. 2025 ASCO Annual Meeting, Chicago, IL. Abstract #3142.