Imunoterapija u onkologiji: koje vrste postoje i gdje je njihova primjena danas
Imunoterapija u onkologiji danas je jedno od najvažnijih i najbrže rastućih područja suvremene medicine. Riječ je o skupini terapijskih pristupa kojima se imunološki sustav potiče, usmjerava ili modulira kako bi učinkovitije prepoznao i uklonio tumorske stanice. Za razliku od klasičnih citotoksičnih oblika liječenja raka, imunoterapija ne djeluje primarno tako da izravno oštećuje tumor, nego tako da aktivira ili pojačava prirodne mehanizme antitumorske imunosti. Upravo zato imunoterapija u onkologiji danas zauzima sve važnije mjesto u liječenju brojnih malignih bolesti.
Prema prikazu Cancer Research Institutea, među glavne vrste imunoterapije ubrajaju se adoptivna stanična terapija, cjepiva protiv raka, imunomodulatori, onkolitička virusna terapija i ciljano usmjerena protutijela. Važno je pritom naglasiti da taj pregled obuhvaća i već odobrene terapijske pristupe i one koji su još predmet kliničkih istraživanja. To najbolje pokazuje koliko je onkologija danas dinamično područje medicine u kojem se terapijske mogućnosti stalno šire.

Adoptivna stanična terapija
Adoptivna stanična terapija jedan je od najnaprednijih oblika imunoterapije u onkologiji. Temelji se na uporabi imunoloških stanica koje se izoliraju iz bolesnika, laboratorijski umnažaju i/ili genski modificiraju te potom vraćaju u organizam s ciljem snažnijeg i preciznijeg antitumorskog djelovanja. Ovaj se pristup često opisuje i kao oblik „živih lijekova”, jer terapijski učinak proizlazi iz funkcionalne aktivnosti živih imunoloških stanica.
Suština ovog pristupa u liječenju raka jest u tome da se postojeći imunološki odgovor protiv tumora ne promatra kao nešto fiksno, nego kao nešto što se može pojačati, preusmjeriti i učiniti učinkovitijim. U tom je smislu adoptivna stanična terapija jedan od najuvjerljivijih primjera personaliziranog liječenja u onkologiji. Cancer Research Institute pritom ističe i da je razvoj ovih terapija dodatno ubrzan napretkom tehnologija genske modifikacije, uključujući CRISPR.
U ovu skupinu imunoterapije ubraja se više različitih pristupa. Terapija tumorski infiltrirajućim limfocitima, odnosno TIL terapija, temelji se na izdvajanju limfocita koji su već prisutni unutar tumorskog tkiva, njihovoj laboratorijskoj ekspanziji te ponovnoj primjeni bolesniku. Time se nastoji pojačati već postojeći, ali često nedovoljno snažan antitumorski odgovor protiv tumora.
Drugi pristup imunoterapiji uključuje T-stanice koje se genski modificiraju tako da izražavaju inženjerski T-stanični receptor, odnosno TCR. Na taj se način T-stanicama omogućuje bolje prepoznavanje određenih tumorskih antigena. Sličnu logiku u onkologiji ima i CAR-T terapija, u kojoj se T-stanice dizajniraju da pomoću himernog antigenskog receptora prepoznaju specifične molekularne mete na tumorskim stanicama.
U adoptivnu staničnu terapiju ubraja se i terapija NK-stanicama, pri kojoj se koriste prirodne stanice ubojice kao efektorske stanice antitumorskog imunološkog odgovora. Prema navedenom izvoru, ovi se pristupi već koriste ili se intenzivno istražuju kod hematoloških maligniteta, poput leukemija i limfoma, ali i kod pojedinih solidnih tumora, uključujući glioblastom. To potvrđuje da imunoterapija širi svoju primjenu i izvan klasičnih indikacija.

Cjepiva protiv raka
Cjepiva protiv raka predstavljaju drugu važnu skupinu imunoterapijskih pristupa u onkologiji. Njihov je cilj imunološkom sustavu prezentirati tumorske ili s tumorom povezane antigene kako bi se potaknuo specifičan antitumorski odgovor usmjeren protiv malignih stanica.
Kada govorimo o cjepivima protiv raka u kontekstu liječenja raka, važno je razlikovati preventivna, terapijska i personalizirana neoantigenska cjepiva. Svaka od tih skupina ima drukčiju ulogu i drukčiji klinički kontekst unutar suvremene onkologije.
Preventivna cjepiva nisu usmjerena protiv već postojećeg tumora, nego protiv infekcija koje mogu povećati rizik razvoja malignih bolesti. Kao najvažniji primjer navodi se HPV cjepivo, koje štiti od sojeva humanog papiloma virusa povezanih s nastankom cervikalnog karcinoma, ali i drugih HPV-povezanih zloćudnih bolesti, uključujući analni, orofaringealni i penilni karcinom. Prema prikazu na stranici, široka primjena HPV cijepljenja povezana je sa smanjenjem incidencije cervikalnog karcinoma, osobito u populacijama s visokom procijepljenošću, što pokazuje preventivni potencijal imunoterapije.
Terapijska cjepiva imaju drukčiju svrhu u onkologiji: primjenjuju se kod već dijagnosticirane maligne bolesti. Kao primjer se navodi sipuleucel-T za uznapredovali rak prostate. Riječ je o personaliziranom postupku u kojem se bolesnikove vlastite imunosne stanice izlažu antigenu povezanom s tumorskim stanicama prostate, s ciljem poticanja ciljanog imunološkog odgovora protiv raka.
Posebno zanimljivo područje razvoja imunoterapije predstavljaju personalizirana neoantigenska cjepiva. Ona se izrađuju na temelju mutacijama nastalih antigena koji su specifični za pojedini tumor i pojedinog bolesnika. Ideja je razviti cjepivo koje će imunološki sustav usmjeriti upravo na one molekularne promjene koje razlikuju tumorsko tkivo od zdravog, čime se nastoji postići visoka specifičnost liječenja raka uz manji utjecaj na zdrave stanice. Rani klinički rezultati, prema prikazu izvora, djeluju obećavajuće u različitim vrstama raka.

Imunomodulatori
Imunomodulatori čine vrlo važnu i široku skupinu lijekova unutar imunoterapije u onkologiji koji djeluju na regulatorne mehanizme imunološkog sustava. Njihova osnovna zadaća nije nužno izravno uništiti tumorsku stanicu, nego pojačati, usmjeriti ili fino podesiti imunološki odgovor tako da postane djelotvorniji protiv tumora.
Cancer Research Institute ovu skupinu imunoterapije dijeli na inhibitore imunoloških kontrolnih točaka, citokine, agoniste i adjuvanse. Svaka od tih podskupina djeluje na drugačiji način, ali im je zajedničko da mijenjaju tumorski mikrookoliš i potencijal imunološkog sustava da odgovori na prisutnost tumora.
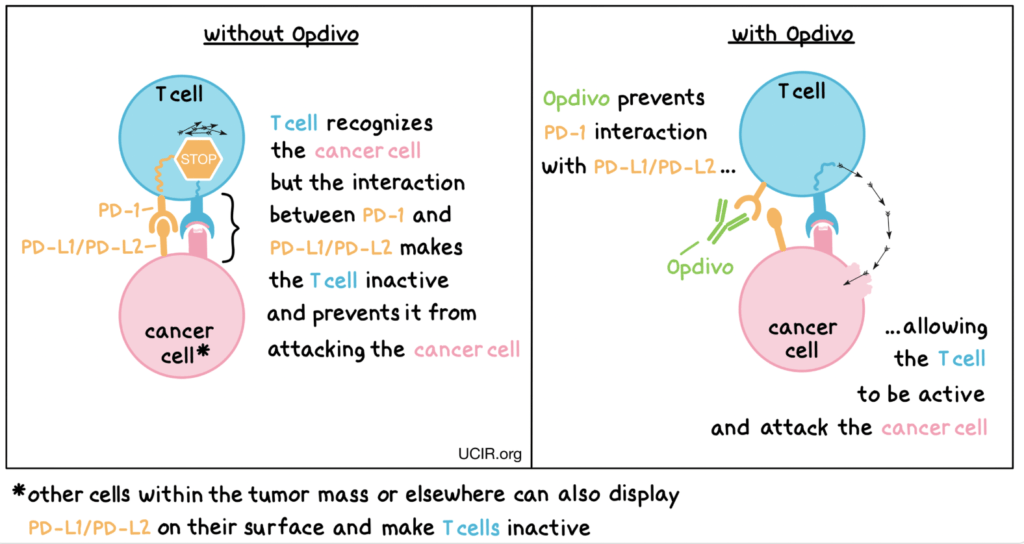
Inhibitori kontrolnih točaka danas su među najvažnijim i najpoznatijim oblicima onkološke imunoterapije. Oni blokiraju proteine koji fiziološki djeluju kao „kočnice” imunološkog odgovora. U tumorskom okruženju te se kočnice često prekomjerno aktiviraju, što tumoru omogućuje izbjegavanje imunološkog nadzora. Blokadom tih mehanizama omogućuje se snažnija T-stanična aktivnost protiv tumora. Kao primjeri se navode nivolumab i pembrolizumab, koji su pokazali učinkovitost u liječenju raka poput melanoma i nemikrocelularnog raka pluća.
Citokini, uključujući interferone i interleukine, predstavljaju drugu skupinu imunomodulatora u imunoterapiji. Oni moduliraju imunološki odgovor i već su korišteni u liječenju bolesti poput melanoma i raka bubrega. Iako se njihova primjena razlikuje od suvremenijih inhibitora kontrolnih točaka, njihova uloga u razvoju onkološke imunoterapije ostaje važna.
Agonisti i adjuvansi u okviru imunoterapije imaju zadaću stimulirati imunološke efektorske stanice i dodatno pojačati antitumorski odgovor, dok adjuvansi služe povećanju imunogenosti, osobito u kontekstu cjepiva. Drugim riječima, oni pomažu imunološkom sustavu da snažnije i učinkovitije odgovori na terapijski poticaj. Stranica pritom naglašava da se broj dostupnih imunomodulatora kontinuirano povećava, što dodatno proširuje terapijske mogućnosti u onkologiji.
Onkolitička virusna terapija
Onkolitička virusna terapija u onkologiji temelji se na uporabi genetski modificiranih virusa koji selektivno inficiraju i razaraju tumorske stanice, uz relativno pošteđivanje zdravog tkiva. Ovaj je pristup posebno zanimljiv jer kombinira dva mehanizma djelovanja: izravno uništavanje tumorskih stanica i poticanje sekundarnog imunološkog odgovora protiv raka.
Tumorske stanice često imaju slabije mehanizme antivirusne obrane od zdravih stanica, što ih čini pogodnijima za selektivnu virusnu infekciju. Kada virus inficira i razori tumorsku stanicu, dolazi do oslobađanja tumorskih antigena, a to dodatno može aktivirati imunološki sustav i pojačati antitumorski odgovor i izvan mjesta primarne infekcije. Upravo zato je ova vrsta imunoterapije važna u suvremenom liječenju raka.
Kao najpoznatiji primjer navodi se talimogene laherparepvec, odnosno T-VEC (Imlygic®), modificirani herpes simplex virus razvijen za liječenje melanoma. Njegov terapijski učinak temelji se na dvostrukom djelovanju: s jedne strane izravno inficira i uništava tumorske stanice, a s druge strane potiče stvaranje GM-CSF-a, čimbenika koji dodatno stimulira imunološki sustav. Uspjeh T-VEC-a u liječenju melanoma otvorio je prostor za razvoj i istraživanje drugih onkolitičkih virusnih platformi za različite vrste raka.

Ciljano usmjerena protutijela
Ciljano usmjerena protutijela predstavljaju važan segment precizne onkologije i imunoterapije. Njihovo djelovanje temelji se na prepoznavanju specifičnih antigena na tumorskim stanicama, ometanju tumorske signalizacije te olakšavanju imunološkog prepoznavanja i uklanjanja malignih stanica.
U ovoj skupini imunoterapije razlikuju se „naked” monoklonska protutijela, konjugati protutijelo-lijek, odnosno ADC, te bispecifična protutijela. Iako svi ti pristupi koriste protutijela kao osnovni terapijski alat, način njihova djelovanja može biti vrlo različit, što dodatno širi mogućnosti liječenja raka.
„Naked” monoklonska protutijela djeluju tako da se vežu za specifične mete na tumorskim stanicama i na taj način ometaju njihovu biološku aktivnost ili olakšavaju njihovo prepoznavanje od strane imunološkog sustava. Kao primjer se navodi trastuzumab u liječenju HER2-pozitivnog raka dojke, što je jedan od klasičnih primjera ciljane terapije u onkologiji.
Konjugati protutijelo-lijek predstavljaju dodatni iskorak u preciznosti liječenja raka. Kod njih protutijelo služi kao nosač citotoksične tvari koja se ciljano dostavlja tumorskoj stanici. Kao primjer se navodi ado-trastuzumab emtansine, koji pokazuje kako imunoterapija i ciljano liječenje mogu biti spojeni u jednom terapijskom konceptu.
Bispecifična protutijela istodobno vežu dvije različite mete. Time mogu, primjerice, funkcionalno približiti T-stanicu tumorskoj stanici i tako omogućiti učinkovitiji imunološki napad. Kao primjer se navodi blinatumomab, koji se koristi u akutnoj limfoblastičnoj leukemiji. Ova skupina terapija vrlo jasno pokazuje u kojem smjeru ide moderna onkologija: prema sve preciznijem, biološki usmjerenom i individualiziranom liječenju raka.

Gdje imunoterapija danas ima najveću kliničku primjenu
Prema prikazu Cancer Research Institutea, imunoterapija u onkologiji pokazala je osobit terapijski učinak u liječenju uznapredovalih oblika raka pluća, melanoma, raka mokraćnog mjehura i raka bubrega. Istodobno, popis malignih bolesti kod kojih se imunoterapija koristi ili istražuje stalno raste. To je posljedica razvoja novih lijekova, boljeg razumijevanja tumorske biologije i sve većeg broja kliničkih ispitivanja u području liječenja raka.
Važno je međutim naglasiti da imunoterapija nije jednako učinkovita kod svih bolesnika ni kod svih vrsta tumora. Unatoč velikom napretku, odgovor na liječenje raka ostaje heterogen i ovisi o više bioloških i kliničkih čimbenika.

Što utječe na odgovor na imunoterapiju
Odgovor na imunoterapiju ovisi o nizu međusobno povezanih čimbenika. Među najvažnijima su histološki tip tumora, mutacijsko opterećenje, ekspresija PD-L1, obilježja tumorskog mikrookoliša, stanje imunološkog sustava bolesnika, prethodno provedena liječenja, genetski čimbenici, opće zdravstveno stanje te mogućnost kombiniranja imunoterapije s drugim terapijskim modalitetima.
Posebno je važno i tumorsko mikrookoliš, koje može biti više ili manje pogodno za aktivan imunološki odgovor. Neki tumori stvaraju snažno imunosupresivno okruženje i time otežavaju djelovanje imunoterapije. Uz to, novija istraživanja upućuju i na moguću povezanost crijevnog mikrobioma s učinkovitošću imunoterapije u onkologiji. Sve to pokazuje koliko je predviđanje odgovora na liječenje složeno i zašto odluka o primjeni imunoterapije mora biti individualizirana.
Tko je kandidat za imunoterapiju
Pitanje prikladnosti za imunoterapiju ne može se svesti na jedno jednostavno pravilo. Prema navedenom izvoru, podobnost za pojedine oblike imunoterapije u onkologiji često ovisi o prethodnim linijama liječenja, prisutnosti specifičnih tumorskih biljega i biološkim obilježjima samog tumora.
Zato procjena prikladnosti imunoterapije zahtijeva individualan pristup i multidisciplinarnu evaluaciju. U kliničkoj praksi odluka o uključivanju imunoterapije u plan liječenja donosi se na temelju vrste bolesti, stadija, molekularnih obilježja tumora, općeg stanja bolesnika i ciljeva liječenja raka.
Zašto je imunoterapija toliko važna u suvremenoj onkologiji
Vrijednost imunoterapije u onkologiji ne leži samo u činjenici da predstavlja novu skupinu lijekova, nego i u tome što je promijenila način na koji razmišljamo o liječenju raka. Umjesto isključivog fokusiranja na izravno uništavanje tumora, sve se više koristi pristup kojim se aktivira vlastiti obrambeni sustav organizma. U odabranih bolesnika to može dovesti do dugotrajnije kontrole bolesti, a razvoj novih terapijskih platformi dodatno proširuje mogućnosti onkološkog liječenja.
Imunoterapija je zato danas jedno od najdinamičnijih područja onkologije. Razvoj staničnih terapija, cjepiva, inhibitora kontrolnih točaka, onkolitičkih virusa i ciljanih protutijela potvrđuje važnost personaliziranog liječenja i otvara prostor za još preciznije i učinkovitije liječenje malignih bolesti u budućnosti.

Zaključak
Imunoterapija u onkologiji danas je jedno od najvažnijih područja suvremenog liječenja raka jer koristi vlastiti imunološki sustav za prepoznavanje i uklanjanje tumorskih stanica. Razvoj različitih pristupa, od adoptivne stanične terapije i cjepiva protiv raka do inhibitora kontrolnih točaka, onkolitičkih virusa i ciljanih protutijela, pokazuje koliko se brzo šire mogućnosti personaliziranog liječenja.
Ipak, imunoterapija nije jednako učinkovita kod svih bolesnika ni kod svih vrsta tumora. Upravo zato njezina primjena zahtijeva individualiziran pristup, pažljivu procjenu bioloških obilježja bolesti i multidisciplinarno donošenje odluka. Unatoč tim ograničenjima, imunoterapija je već bitno promijenila ishode liječenja u nizu malignih bolesti i ostaje jedno od najperspektivnijih područja suvremene onkologije.
Imunoterapija ukratko
Imunoterapija
- Imunoterapija je skup suvremenih onkoloških terapija koje aktiviraju, usmjeravaju ili moduliraju imunološki sustav kako bi učinkovitije prepoznao i uklonio tumorske stanice.
- Za razliku od klasičnih citotoksičnih terapija, ne djeluje primarno izravnim oštećenjem tumora, nego poticanjem prirodnih mehanizama antitumorske imunosti.
- Danas predstavlja jedno od najdinamičnijih područja onkologije i važan dio razvoja personaliziranog liječenja malignih bolesti.
Glavne vrste imunoterapije
- Glavne vrste imunoterapije uključuju:
- adoptivnu staničnu terapiju
- cjepiva protiv raka
- imunomodulatore
- onkolitičku virusnu terapiju
- ciljano usmjerena protutijela
Adoptivna stanična terapija
- Temelji se na izolaciji, laboratorijskom umnažanju i/ili genskoj modifikaciji imunoloških stanica koje se potom vraćaju bolesniku radi snažnijeg antitumorskog djelovanja.
- U ovu skupinu ubrajaju se:
- TIL terapija
- TCR terapija
- CAR-T terapija
- terapija NK-stanicama
- Ovi se pristupi već koriste ili se intenzivno istražuju kod:
- hematoloških maligniteta poput leukemija i limfoma
- nekih solidnih tumora, uključujući glioblastom
Cjepiva protiv raka
- Cjepiva protiv raka imaju cilj imunološkom sustavu prezentirati tumorske ili s tumorom povezane antigene kako bi se potaknuo specifičan antitumorski odgovor.
- Razlikuju se:
- preventivna cjepiva
- terapijska cjepiva
- personalizirana neoantigenska cjepiva
Preventivna cjepiva
- Preventivna cjepiva, poput HPV cjepiva, smanjuju rizik razvoja određenih malignih bolesti povezanih s infekcijama.
- To uključuje:
- cervikalni karcinom
- analni karcinom
- orofaringealni karcinom
- penilni karcinom
Terapijska cjepiva
- Terapijska cjepiva primjenjuju se kod već dijagnosticirane zloćudne bolesti.
- Primjer je sipuleucel-T za uznapredovali rak prostate.
Personalizirana neoantigenska cjepiva
- Razvijaju se na temelju mutacijama nastalih antigena specifičnih za pojedinog bolesnika i njegov tumor.
Imunomodulatori
- Imunomodulatori su lijekovi koji pojačavaju, usmjeravaju ili reguliraju imunološki odgovor protiv tumora.
- U ovu skupinu ubrajaju se:
- inhibitori imunoloških kontrolnih točaka
- citokini
- agonisti
- adjuvansi
Inhibitori kontrolnih točaka
- Lijekovi poput nivolumaba i pembrolizumaba blokiraju mehanizme koji koče imunološki odgovor.
- Time omogućuju snažniju T-staničnu aktivnost protiv tumora.
Citokini
- Citokini, uključujući interferone i interleukine, koriste se za modulaciju imunološkog odgovora.
- Primjenjuju se, primjerice, u liječenju melanoma i raka bubrega.
Agonisti i adjuvansi
- Agonisti dodatno stimuliraju imunološke stanice.
- Adjuvansi povećavaju imunogenost i mogu pojačati učinak cjepiva.
Onkolitička virusna terapija
- Ova terapija koristi genetski modificirane viruse koji selektivno inficiraju i razaraju tumorske stanice, uz relativno pošteđivanje zdravog tkiva.
- Osim izravnog uništavanja tumora, može potaknuti i sekundarni imunološki odgovor oslobađanjem tumorskih antigena.
- Najpoznatiji primjer je T-VEC (Imlygic®), modificirani herpes simplex virus koji se koristi u liječenju melanoma.
Ciljano usmjerena protutijela
- Djeluju tako da prepoznaju specifične antigene na tumorskim stanicama, ometaju tumorsku signalizaciju i olakšavaju imunološko uklanjanje malignih stanica.
- U ovu skupinu ubrajaju se:
- „naked” monoklonska protutijela
- konjugati protutijelo-lijek (ADC)
- bispecifična protutijela
- Primjeri uključuju:
- trastuzumab
- ado-trastuzumab emtansine
- blinatumomab
Gdje imunoterapija pokazuje osobit učinak
- Imunoterapija je pokazala osobit učinak kod:
- uznapredovalog raka pluća
- melanoma
- raka mokraćnog mjehura
- raka bubrega
- Broj indikacija i dalje raste.
Što utječe na odgovor na imunoterapiju
- Odgovor na imunoterapiju nije jednak kod svih bolesnika.
- Ovisi o više čimbenika, uključujući:
- histološki tip tumora
- mutacijsko opterećenje
- PD-L1 ekspresiju
- tumorsko mikrookruženje
- prethodno liječenje
- genetske čimbenike
- opće stanje bolesnika
- Sve se više istražuje i moguća povezanost crijevnog mikrobioma s učinkovitošću imunoterapije.
Klinički pristup
- Odluka o primjeni imunoterapije zahtijeva:
- individualiziran pristup
- multidisciplinarnu procjenu
Kratak pregled terapija po skupinama
Adoptivna stanična terapija
Obuhvaća TIL terapiju, TCR terapiju, CAR-T terapiju i terapiju NK-stanicama. Temelji se na izolaciji, umnažanju i/ili genskoj modifikaciji imunoloških stanica radi pojačanog antitumorskog učinka.
Cjepiva protiv raka
Uključuju preventivna cjepiva, terapijska cjepiva i personalizirana neoantigenska cjepiva. Njihov je cilj potaknuti specifičan imunološki odgovor protiv infekcija povezanih s rakom ili protiv samih tumorskih antigena.
Imunomodulatori
Obuhvaćaju inhibitore kontrolnih točaka, citokine, agoniste i adjuvanse. Djeluju tako da pojačavaju, usmjeravaju ili reguliraju imunološki odgovor protiv tumora.
Onkolitička virusna terapija
Koristi genetski modificirane viruse koji selektivno inficiraju i razaraju tumorske stanice, uz dodatno poticanje sekundarnog imunološkog odgovora.
Ciljano usmjerena protutijela
Uključuju „naked” monoklonska protutijela, konjugate protutijelo-lijek i bispecifična protutijela. Njihovo djelovanje temelji se na preciznom prepoznavanju tumorskih meta i olakšavanju imunološkog uklanjanja malignih stanica.